Поверхностное натяжение равно. Поверхностное натяжение
Вологодский государственный педагогический университет
Курсовая работа по теме :
МЕТОДЫ ИЗМЕРЕНИЯ КОЭФФИЦИЕНТА ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ.
Выполнил : Орехов Н.В.
Вологда 1998
Коэффициент поверхностного натяжения.
Поверхность жидкости, соприкасающейся с другой средой, например с ее собственным паром, с какой-либо другой жидкостью или с твердым телом (в частности, со стенками сосуда, в котором она содержится), находится в особых условиях по сравнению с остальной массой жидкости.
Возникают эти особые условия потому, что молекулы пограничного слоя жидкости, в отличие от молекул в ее глубине, окружены молекулами той же жидкости не со всех сторон. Часть «соседей» поверхностных молекул - это частицы второй среды, с которой жидкость граничит. Она, эта среда, может отличаться от жидкости как природой, так и плотностью частиц. Имея же разных соседей, молекулы поверхностного слоя и взаимодействуют с ними различным образом. Поэтому силы, действующие на каждую молекулу в этом слое, оказываются неуравновешенными: существует некоторая равнодействующая сила, направленная либо в сторону объема жидкости, либо в сторону объема граничащей с ней среды. Вследствие этого перемещение молекулы из поверхностного слоя в глубь жидкости или в глубь среды, с которой она граничит, сопровождается совершением работы (внутри жидкости молекулы, со всех сторон окруженные точно такими же частицами, находятся в равновесии, и их перемещение истребует затраты работы Величина и знак этой работы зависят от соотношения между силами взаимодействия молекул поверхностного слоя со «своими» же молекулами и с молекулами второй среды.
В случае, если жидкость граничит со своим собственным паром (насыщенным), т. е. в случае, когда мы имеем дело с одним веществом, сила, испытываемая молекулами поверхностного слоя, направлена внутрь жидкости. Это объясняется тем, что плотность молекул в жидкости много больше, чем в насыщенном паре над "жидкостью (вдали от критической температуры), и поэтому сила притяжения, испытываемая молекулой поверхностного слоя со стороны молекул жидкости, больше, чем со стороны молекул пара.
Отсюда следует, что, перемещаясь из поверхностного слоя внутрь жидкости, молекула совершает положительную работу. Наоборот, переход молекул из объема жидкости к поверхности сопровождается отрицательной работой, т. е. требует затраты внешней работы.
Представим себе, что по тем или иным причинам поверхность жидкости увеличивается (растягивается). Это значит, что некоторое количество молекул переходит из объема жидкости в поверхностный слой. Для этого, как мы только что видели, надо затратить внешнюю работу. Другими словами, увеличение поверхности жидкости сопровождается отрицательной работой. Наоборот, при сокращении поверхности совершается положительная работа.
Если при постоянной температуре обратимым путем изменить поверхность жидкости на бесконечно малую величину dS , то необходимая для этого работа
| (1) |
Знак минус указывает на то, что увеличение поверхности ( dS > 0) сопровождается отрицательной работой.
Коэффициент
является основной величиной, характеризующей свойства поверхности жидкости, и называется коэффициен том поверхностного натяжения ( > 0). Следовательно, коэффициент поверхностного натяжения измеряется работой, необходимой для увеличения площади поверхности жидкости при постоянной температуре на единицу.Очевидно, в системе СИ
имеет размерность .Из сказанного ясно, что молекулы поверхностного слоя жидкости обладают избыточной по сравнению с молекулами, находящимися в объеме жидкости, потенциальной энергией. Обозначим ее
. Эта энергия, как всегда, измеряется работой, которую могут совершить молекулы поверхности, перемещаясь внутрь жидкости под действием сил притяжения со стороны молекул в объеме жидкости.Поскольку энергия
обязана своим происхождением наличию поверхности жидкости, то она должна быть пропорциональна площади S поверхности жидкости:| (2) |
Тогда изменение площади поверхности dS повлечет за. собой изменение потенциальной энергии
которое сопровождается работой
в полном соответствии с (1).
Если, как было указано, изменение поверхности S осуществляется при постоянной температуре, т. е. изотермически (и обратимо), то, как известно, потребная для этого работа равна изменению свободной энергии F поверхности:
.(Если изменение поверхности жидкости произвести адиабатно, то ее температура изменится. Например, увеличение поверхности приведет к ее охлаждению.) Значит, избыточная потенциальная энергия поверхности жидкости, о которой говорилось выше, является свободной энергией поверхности и, следовательно,
| (3) |
т. е. коэффициент поверхностного натяжения жидкости можно определить как свободную энергию единицы площади этой поверхности.
Теперь ясно, в чем заключаются указанные выше особые условия, в которых находится поверхность жидкости. Они заключаются в том, что поверхность жидкости обладает избыточной по сравнению с остальной массой жидкости потенциальной (свободной) энергией. Посмотрим, к чему это приводит.
Известно, что всякая система при равновесии находится в том из возможных для нее состояний, при котором ее энергия имеет минимальное значение. Применительно к рассматриваемому случаю это означает, что жидкость в равновесии должна иметь минимально возможную поверхность. Это в свою очередь означает, что должны существовать силы, препятствующие увеличению поверхности жидкости, т. е. стремящиеся сократить эту поверхность.
Очевидно, что эти силы должны быть направлены вдоль самой поверхности, по касательной к ней. Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, сокращающие (стягивающие) эту поверхность. Эти силы называются силами поверхностного натяжения.
Нужно, однако, помнить, что первопричиной возникновения сил поверхностного натяжения являются силы, испытываемые молекулами поверхностного слоя, направленные внутрь жидкости, а в некоторых случаях внутрь той среды, с которой она граничит, т. е. перпендикулярно к поверхности.
Для разрыва, или, как говорят, для раздела поверхности необходимо приложить внешние силы, параллельные к поверхности и перпендикулярные к той линии, вдоль которой предполагается разрыв (раздел).
 |
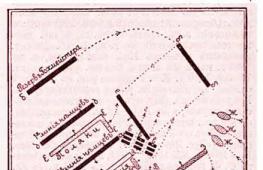
Это особенно ясно видно из опытов с тонкими пленками жидкости. Некоторые Жидкости, как, например, мыльная вода, сапонин и др., обладают свойством образовывать тонкие пленки. Если, например, опустить проволочную рамку, одна из сторон которой подвижна (рис. 1), в мыльный раствор, то вся она затянется пленкой жидкости. Силы поверхностного натяжения принуждают пленку сокращаться, и подвижная перекладина АВ вслед за пленкой перемещается вверх. Чтобы сохранить ее в равновесии, к перекладине нужно приложить силу Р в виде груза (сюда входит и вес самой перекладины).
Таким образом, сила поверхностного натяжения, действующая в пленке, перпендикулярна к линии АВ , которая в данном случае и является линией раздела. Такие же силы действуют, конечно, и на другие стороны рамки. Но здесь они уравновешиваются силами притяжения жидкости к.веществу жесткой рамки.
Описанный опыт может быть использован для определения численного значения коэффициента поверхностного натяжения жидкости, образующей пленку. Действительно, поверхностная сила f , с учетом того, что пленка имеет две поверхности (ведь пленка на самом деле представляет собой тонкий слой жидкости), равна при равновесии весу груза Р :
Если под действием этой силы перекладина, увлекаемая пленкой, переместилась на расстояние dh из положения АВ , та работа, совершенная силой, равна.
Вы видите его проявление всякий раз, когда наблюдаете, как вода медленно капает из водопроводного крана. Из крана появляется водяная пленка и начинает растягиваться, словно тонкая резиновая оболочка, под тяжестью заключенной в ней жидкости. Эта пленка, прикрепленная к отверстию крана, постепенно удлиняется, пока ее вес не станет вдруг слишком большим. Пленка, однако, не рвется, как порвалась бы резника при перегрузке. Вместо этого она "соскальзывает" с копчика крана и, как бы охватив небольшое количество воды, образует свободно падающую капельку. Несомненно, вы не раз наблюдали, что падающие капельки принимают почти шарообразную форму. Если бы не было внешних сил, они были бы строго шарообразны. То, что вы наблюдаете, является одним из проявлений необычной способности воды "стягиваться", "самоуплотняться", или, другими словами, ее способность к сцеплению (когезии). Капля воды, капающая из крана, стягивается в крошечный шар, а шар из всех возможных геометрических тел обладает наименьшей поверхностью при данном объеме.Вследствие сцепления на поверхности воды образуется натяжение, и для того, чтобы разорвать поверхность воды, требуется физическая сила, причем, как это ни странно, довольно значительная. Ненарушенная водная поверхность может удерживать на себе предметы, которые значительно "тяжелее" воды, например стальную иголку или лезвие бритвы, или некоторых насекомых, которые скользят по воде, словно это не жидкость, а твердое тело.

Из всех жидкостей, кроме ртути, у воды самое большое поверхностное натяжение.
Внутри жидкости притяжение молекул друг к другу уравновешено. А на поверхности нет. Молекулы воды, которые лежат глубже, тянут вниз самые верхние молекулы. Поэтому капля воды как бы стремится максимально сжаться. Стягивают ее силы поверхностного натяжения.
Физики точно рассчитали, какую гирю надо подвесить к столбику воды толщиной в три сантиметра, чтобы разорвать его. Гиря потребуется огромная - больше ста тонн! Но это когда вода исключительно чистая. В природе такой воды нет. Всегда в ней что-то растворено. Пусть хоть немного, но чужеродные вещества разрывают звенья в прочной цепи молекул воды, и силы сцепления между ними уменьшаются.
Если нанести на стеклянную пластинку капли ртути, а на парафиновую - капли воды, то очень маленькие капельки будут иметь форму шара, а более крупные окажутся слегка сплюснутыми под действием силы тяжести.

Подобное явление объясняется тем, что между ртутью и стеклом, а также между парафином и водой возникают силы притяжения (адгезия) меньшие чем между самими молекулами (когезия). При соприкосновении воды с чистым стеклом, а ртути с металлической пластинкой мы наблюдаем почти равномерное распределение того и другого вещества на пластинках, так как силы притяжения между стеклом и молекулами воды, металлом и молекулами ртути больше, чем притяжение между отдельными молекулами воды и ртути. Такое явление, когда жидкость равномерно располагается на поверхности твёрдого тела, называется смачиванием. Значит, вода смачивает чистое стекле, но не смачивает парафин. Смачиваемость в частном случае может показать степень загрязнённости поверхности. Например, на чисто вымытой тарелке (фарфоровой, фаянсовой) вода растекается ровным слоем, в чисто вымытой колбе стенки равномерно покрываются водой, если же вода на поверхности принимает форму капель, то это указывает, что поверхность посуды покрыта тонким слоем вещества, которое не смачивает вода, чаще всего жиром.
вода
Рис. 12.1
воздух
Лекция 12. Поверхностное натяжение жидкостей. Осмос
В этой лекции рассмотрим некоторые свойства жидкостей, связанные с поведением молекул в жидкой фазе. В отличие от практически свободных и быстрых молекул газа молекулы жидкости расположены вплотную друг к другу и перемещаются довольно медленно.
12.1. Поверхностное натяжение жидкостей
Упругими свойствами обладают не только твердые тела, но и поверхность жидкости. Каждый видел, как растягивается мыльная пленка при выдувании пузырей. Силы поверхностного натяжения, возникающие в мыльной пленке, удерживают воздух в пузыре, подобно тому, как растянувшаяся резиновая камера удерживает воздух в футбольном мяче.
Поверхностное натяжение возникает на границе раздела фаз, например, жидкой и газообразной или жидкой и твердой, и обусловлено тем, что молекулы поверхностного слоя жидкости испытывают разную силу притяжения снаружи и изнутри. Поверхностное на-
Тяжение хорошо наблюдать на примере капли воды, где
жидкость ведет себя так, как будто она помещена в эла-
стичную оболочку. Здесь молекулы поверхностного слоя воды притягиваются к своим внутренним соседям (другим молекулам воды) сильнее, чем к внешним молекулам воздуха, рис. 12.1. Другой пример – пленка бензина на воде. Здесь молекулы бензина притягиваются друг к
другу слабее, чем к молекулам воды, в результате чего бензин растекается по воде очень тонкой пленкой.
Поверхностное натяжение можно определить как бесконечно малую (элементарную) работу δ A , которую нужно совершить для увеличения площади поверхности жидкости на бесконечно малую величину dS при постоянной тем-
определяет упругие свойства поверхности жидкости. Чем больше поверхностное натяжение, тем труднее растягивается пленка жидкости.
Поверхностное натяжение зависит от температуры . Например, для воды с ростом температуры поверхностное натяжение уменьшается.
Сила поверхностного натяжения F пропорциональна длине контура l на поверхности, к которому приложена, и лежит в плоскости, касательной к по-
верхности жидкости, |
|
F = σ l. |
Жидкость может смачивать или не смачивать поверхность, на которую она налита. Если молекулы жидкости притягиваются друг к другу слабее, чем к

0 ≤ θ < π /2 |
π/2 < θ ≤ π |
||||||||||||
молекулам поверхности, происходит смачивание (рис. 12.2, а), в противном случае – несмачивание (рис. 12.2, б).
Угол, образованный поверхностью, куда налита жидкость, и касательной к поверхности жидкости, называется краевым углом θ . Предельный случай, когда θ = 0, называется полным смачиванием, а когда θ = π , – полным несмачиванием.
Силы поверхностного натяжения искривляют поверхность жидкости и вызывают дополнительное давление, которое определяется формулой Лапласа
P = σ |
||||||||
и действует в сторону вогнутости поверхности. Здесь R 1 и R 2 − радиусы кри- |
||||||||
визны двух взаимно перпендикулярных сечений поверхности жидкости. |
||||||||
Если поверхность цилиндрическая (R 1 = R , R 2 → ∞ ), то |
||||||||
σ , |
(12.3)′ |
|||||||
если сферическая (R 1 = R 2 = R ), то |
||||||||
(12.3)″ |
||||||||
Искривленная поверхность жидкости называется мениском . Поверхностное натяжение проявляется и в случае поднятия жидкости в
капиллярных трубках (рис. 12.3, а). Например, в капиллярах стеблей травянистых растений за счет смачивания вода поднимается на несколько сантиметров. Высота поднятия жидкости с плотностью ρ в капиллярной трубке1 радиуса r
Капиллярные явления играют важную роль в природе и сельскохозяйственной практике. Как уже отмечалось, вода по капиллярам поднимается в стеб-
1 Мениск в капиллярах сферический и дополнительное давление определяется формулой (12.3)″ . Дополнительное давление как бы затягивает жидкость наверх. Это давление уравновешивается гидростатическим давлением столбика жидкости высоты h : P = ρ gh . Учитывая, что радиус кривизны поверхности R связан с радиусом капилляра r соотношением R = r /cosθ , получим формулу (12.4).

ли травянистых растений. По капиллярам почвы вода поднимается из глубинных в поверхностные слои. Уменьшая диаметр почвенных капилляров путем уплотнения почвы, можно усилить приток воды к поверхности, то есть к зоне испарения, и этим ускорить высушивание почвы. Наоборот, разрыхляя поверхность почвы и создавая тем самым прерывистость в системе почвенных капилляров, можно задержать приток воды к зоне испарения и замедлить высушивание почвы. На этом основаны агротехнические приемы регулирования водного режима почвы: прикатка и боронование.
Следует также отметить, что пчелы извлекают нектар из цветка посредством очень тонкой капиллярной трубки, находящейся внутри пчелиного хоботка.
Если пузырек воздуха попадет в кровеносный сосуд небольшого диаметра, то из-за сил поверхностного натяжения может наступить закупорка сосуда (пузырек как бы прилипает к стенкам сосуда и перекрывает его). Это явление называется газовой эмболией . Поэтому при инъекциях нельзя допускать попадания в иглу шприца пузырьков воздуха. Для этого перед инъекцией всегда сбрасывают немного жидкости из шприца.
Кроме того, листья и плоды многих растений не смачиваются водой (покрытывосковымналетом), что предохраняет их отзагниваниявдождливыепериоды.
Оперение водоплавающих птиц предохраняется от намокания следующим образом. Плотное переплетение перьевых и пуховых бородок образует упорядоченную структуру. Жирные выделения расположенной у основания хвоста копчиковой железы, наносимые клювом на перья, сохраняют эту структуру и создают водоотталкивающую (несмачивающуюся) поверхность. Водонепроницаемости также способствуют многочисленные пузырьки воздуха, заключенные в тончайших полостях слоев оперения.
В заключение отметим, что для уменьшения поверхностного натяжения воды используют различные поверхностно-активные вещества (ПАВ), например, мыло. Вода не смачивает (и не отмывает) жирную поверхность, а мыльный раствор – смачивает (и отмывает).
12.2. Осмос и осмотическое давление
Это явление похоже на диффузию, однако, одно существенное отличие заставляет рассматривать его отдельно. Для протекания этого явления необходима перегородка (оболочка), обладающая избирательной проницаемостью , то есть пропускающая одни молекулы и не пропускающая другие.
Пусть водный раствор какого-либо вещества, на- |
|||||||||
пример, сахара, отделен от растворителя, например, воды, |
|||||||||
р-р сахара |
|||||||||
полупроницаемой перегородкой, через которую молекулы |
|||||||||
Р осм |
воды проходить могут, а сахара – нет (рис. 12.4). Приме- |
||||||||
рами полупроницаемых перегородок могут служить обо- |
|||||||||
лочка растительной или животной клетки, защитная обо- |
|||||||||
лочка, покрывающая жаберные лепестки рыб, стенки |
|||||||||
желчного пузыря, кишечная ткань и т.д. |
|||||||||

Явление перехода молекул чистого растворителя через полупроницаемую перегородку в область, занятую раствором, называется осмосом .
В результате этого возникает разность давлений между раствором и чистым растворителем. Когда она достигнет определенного значения, осмос прекращается. Разность давлений, при которой осмос прекращается, называется
осмотическим давлением.
Природа осмотического давления будет понятна, если растворенное вещество рассматривать как идеальный газ с молярной концентрацией n р (для слабых растворов).
Р осм = n рRT , |
где n р = ν /V – молярная концентрация раствора в моль/м3 . Это уравнение полностью совпадает с уравнением Менделеева – Клапейрона для газов, только вместо молекул газа здесь молекулы или ионы растворенного вещества.
Осмотическое давление легко измерить. Для этого |
||||||||||
можно провести опыт с поднятием раствора сахара в труб- |
||||||||||
ке, закрытой снизу полупроницаемой перегородкой и по- |
||||||||||
груженной в воду, как показано на рис. 12.5. Из-за осмоса |
||||||||||
молекулы воды будут проходить через перегородку, уро- |
||||||||||
вень в трубке начнет расти и остановится, когда гидроста- |
||||||||||
тическое давление столба жидкости в трубке не даст моле- |
||||||||||
кулам воды проходить в раствор (другими словами, осмо- |
перегородка |
|||||||||
тическое давление в растворе уравновешивается гидроста- |
||||||||||
тическим давлением столба раствора высоты h ). Высота |
||||||||||
подъема раствора в трубке служит мерой осмотического давления |
||||||||||
Р осм = ρ рgh , |
||||||||||
где ρ р – плотность раствора (для слабых растворов примерно равна плотности чистого растворителя). Формула (12.6) – экспериментальная формула для определения осмотического давления.
Осмотический эффект играет исключительно важную роль в жизни бактерий, грибов, растений и животных, так как благодаря осмосу происходит водный обмен клетки с внеклеточной жидкостью. Оболочки живых клеток представляют собой полупроницаемые перегородки, – они проницаемы для молекул воды и непроницаемы для молекул сложных органических соединений, образующихся внутри клетки в процессе ее жизнедеятельности. Благодаря этому внутри клетки образуется раствор с концентрацией несколько превышающей концентрацию внеклеточного раствора, и возникает осмотическое давление, растягивающее клеточную мембрану и делающее клетку упругой, как надутый резиновый мяч. Это явление называется тургором клеток. Поэтому ткани растений и животных обладают хорошей упругостью и сохраняют свою форму. Падение осмотического давления в клетках, например, при обезвоживании организма, приводит к их коллапсу (схлопыванию). А обессоливание организма, наоборот, может привести к набуханию и разрыву клеток (осмотический шок).
Если слегка увядшие растения положить в ванну с холодной водой, то благодаря осмосу, они «оживут». Вода будет проходить через мембраны «подсохших» клеток и вернет им прежнюю форму. Осмотическое давление в расти-
тельных клетках, окруженных водой, может быть весьма значительным и достигать нескольких атмосфер. Именно благодаря осмосу вода из почвы попадает в клетки листьев очень высоких деревьев. Так, эвкалипты и секвойи достигают высоты 100-120 м. Концентрация клеточного раствора в листьях таких растений достаточно высокая, значит, и высокое осмотическое давление (12.5), следовательно, и большая высота подъема воды (12.6).
Если же, растение или животное находятся в растворе с концентрацией, превышающей клеточную концентрацию, то вода идет из клеток во внешний раствор. Например, когда мы делаем варенье и засыпаем фрукты сахаром, образуется сироп – раствор сахара в воде, вышедшей из клеток фруктов. Аналогичный процесс происходит и при засолке рыбы или овощей.
Благодаря осмосу речным рыбам не нужно пить, – вода поступает в ткани не только через желудок, но и через всю внешнюю поверхность рыбы. Так что пресноводным рыбам нужно постоянно выводить избыток воды. А у морских рыб, кроме акул и скатов, концентрация клеточного раствора меньше концентрации солей в морской воде, и они вынуждены пить воду, усваивая ее через желудок. Море в прямом смысле «высасывает» воду из тканей рыб. Кстати, именно осмотическим высасыванием воды из клеток обусловлено чувство жажды, возникающее после приема соленой пищи или питья морской воды.
Кроме того, с ростом концентрации раствора (а, значит, и осмотического давления) уменьшается температура его замерзания. По этой причине почки растений и ткани некоторых животных зимой полностью не промерзают (некоторые виды рыб выдерживают полное промерзание водоема, не зарываясь в ил). Морская вода не замерзает при температурах до –2 ° С и ниже в зависимости от солености.
Напротив, температура кипения раствора с ростом концентрации (а, значит, и осмотического давления) увеличивается. Поэтому температура кипения соленой воды при атмосферном давлении выше 100 ° С.
Причины изменения температуры плавления и кипения воды в зависимости от давления рассмотрены в предыдущей лекции.
Вопросы к лекции 12
1. Как возникает поверхностное натяжение жидкостей? Приведите примеры.
2. Как определяется коэффициент поверхностного натяжения жидкости, и от чего он зависит?
3. Поясните, в каком случае жидкость смачивает поверхность, с которой соприкасается, а в каком – нет.
4. При взятии крови для анализа используется тонкая капиллярная трубка. Почему кровь «сама» поднимается по капилляру? Почему такого эффекта практически не наблюдается, если трубка не достаточно тонкая?
5. Почему при инъекциях нельзя допускать попадания в иглу шприца пузырьков воздуха?
6. Приведите примеры капиллярных явлений в жизни растений и животных.
7. Что такое осмос? Как найти осмотическое давление?
8. Приведите примеры осмотического эффекта в живых организмах.
9. Объясните механизм подъема воды в листья высоких деревьев.
10. Почему мы хотим пить после приема соленой пищи? Почему от сладкой пищи чувство жажды гораздо меньше?
ОПРЕДЕЛЕНИЕ
Поверхностное натяжение - стремление жидкости сократить свою свободную поверхность, т.е. уменьшить избыток своей потенциальной энергии на границе раздела с газообразной фазой.
Опишем механизм возникновения поверхностного натяжения в жидкостях. Жидкость, в отличие от газов, не заполняет весь объем сосуда, в который она налита. Между жидкостью и газом (или паром) образуется граница раздела, которая находится в особых условиях по сравнению с остальной массой жидкости. Рассмотрим две молекулы A и B. Молекула A находится внутри жидкости, молекула B - на ее поверхности (рис. 1). Молекула A окружена другими молекулами жидкости равномерно, поэтому силы, действующие на молекулу A со стороны молекул, попадающих в сферу межмолекулярного взаимодействия, скомпенсированы, или, другими словами, их равнодействующая равна нулю. Молекула B с одной стороны окружена молекулами жидкости, а с другой стороны - молекулами газа, концентрация которых значительно ниже, чем концентрация молекул жидкости. Так как со стороны жидкости на молекулу B действует гораздо больше молекул, чем со стороны газа, равнодействующая всех межмолекулярных сил уже не будет равна нулю и будет направлена внутрь объема жидкости. Таким образом, для того чтобы молекула из глубины жидкости попала в поверхностный слой, нужно совершить работу против не скомпенсированных межмолекулярных сил. А это означает, что молекулы приповерхностного слоя, по сравнению с молекулами внутри жидкости, обладают избыточной потенциальной энергией, которая называется поверхностной энергией .
Очевидно, чем больше площадь поверхности жидкости, тем больше таких молекул, которые обладают избыточной потенциальной энергией, а значит тем больше поверхностная энергия. Этот факт можно записать в виде следующего соотношения:
где поверхностная энергия жидкости, площадь свободной поверхности жидкости и коэффициент пропорциональности, который называется коэффициентом поверхностного натяжения.
Коэффициент поверхностного натяжения
ОПРЕДЕЛЕНИЕ
Коэффициент поверхностного натяжения - это физическая величина, которая характеризует данную жидкость и численно равна отношению поверхностной энергии к площади свободной поверхности жидкости:
Единицей измерения коэффициента поверхностного натяжения в системе СИ является .
Коэффициент поверхностного натяжения жидкости зависит: 1) от природы жидкости (у «летучих жидкостей таких, как эфир, спирт, бензин, коэффициент поверхностного натяжения меньше, чем у «нелетучих - воды, ртути); 2) от температуры жидкости (чем выше температура, тем меньше поверхностное натяжение); 3) от свойств газа, который граничит с данной жидкостью; 4) от наличия поверхностно-активных веществ таких, как мыло или стиральный порошок, которые уменьшают поверхностное натяжение. Также следует отметить, что коэффициент поверхностного натяжения не зависит от площади свободной поверхности жидкости .
Из механики известно, что равновесным состояниям системы соответствует минимальное значение ее потенциальной энергии. Вследствие поверхностного натяжения жидкость всегда принимает форму с минимальной поверхностью. Если на жидкость не действуют другие силы или их действие мало, жидкость будет стремиться принимать форму сферы, как, например, капля воды, мыльный пузырь. Также будет вести себя вода в невесомости. Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, сокращающие (стягивающие) эту поверхность. Эти силы называютсясилами поверхностного натяжения .
Поэтому коэффициент поверхностного натяжения можно также определить как модуль силы поверхностного натяжения, действующей на единицу длины контура, ограничивающего свободную поверхность жидкости:
Наличие сил поверхностного натяжения делает поверхность жидкости похожей на упругую растянутую пленку, с той только разницей, что упругие силы в пленке зависят от площади ее поверхности (т.е. от того, как пленка деформирована), а силы поверхностного натяженияне зависятот площади поверхности жидкости. Если положить швейную иглу на поверхность воды, поверхность прогнется и не даст ей утонуть. Действием сил поверхностного натяжения можно объяснить скольжение легких насекомых таких, например, как водомерки, по поверхности водоемов (рис.2). Лапка водомерки деформирует водную поверхность, увеличивая тем самым ее площадь. Вследствие этого возникает сила поверхностного натяжения, которая стремится уменьшить подобное изменение площади. Равнодействующая сил поверхностного натяжения будет направлена вверх, компенсируя при этом силу тяжести.

На действии сил поверхностного натяжения основан принцип действия пипетки (рис.3). Капелька, на которую действует сила тяжести, вытягивается вниз, тем самым увеличивая площадь своей поверхности. Естественно, возникают силы поверхностного натяжения, равнодействующая которых противоположна направлению силы тяжести, и которые не дают капельке растягиваться. При нажатии на резиновый колпачок пипетки, создается дополнительное давление, которое помогает силе тяжести, в результате чего капля падает вниз.

Примеры решения задач
ПРИМЕР 1
| Задание | Тонкое алюминиевое кольцо радиусом 7,8 см соприкасается с мыльным раствором. Каким усилием можно оторвать кольцо от раствора? Температуру раствора считать комнатной. Масса кольца 7 г. |
| Решение | Выполним рисунок.
На кольцо действуют следующие силы: сила тяжести , сила поверхностного натяжения и внешняя сила . Так как кольцо соприкасается с раствором и внешней и внутренней сторонами, то сила поверхностного натяжения равна: Длина контура, ограничивающего поверхность жидкости в данном случае равна длине окружности кольца: С учетом последнего сила поверхностного натяжения: Условие отрыва кольца от поверхности раствора имеет вид: Из таблиц коэффициент поверхностного натяжения мыльного раствора при комнатной температуре . Ускорение свободного падения Переведем единицы в систему СИ: радиус кольца масса кольца кг. Вычислим: |
| Ответ | Для того, чтобы оторвать кольцо от раствора. необходимо приложить силу 0,11 Н. |
ПРИМЕР 2
| Задание | Какое количество энергии освобождается при слиянии мелких водяных капель радиусом мм в одну каплю радиусом 2 мм? |
| Решение | Изменение потенциальной энергии поверхностного слоя капель, обусловленное уменьшением площади поверхности капель при их слиянии в одну каплю равно:
где площадь поверхности всех мелких капель, площадь поверхности большой капли, коэффициент поверхностного натяжения воды. Очевидно, что: где r — радиус маленькой капли, R — радиус большой капли, n — количество маленьких капель. Масса маленькой капли:
масса большой капли:
Так как маленькие капли сливаются в одну большую каплю, можно записать:
откуда количество маленьких капель: а площадь поверхности всех маленьких капель:
Теперь найдем количество энергии, которое освобождается при слиянии капель: Из таблиц коэффициент поверхностного натяжения воды . Переведем единицы в систему СИ: радиус маленькой капли радиус большой капли . Вычислим: |
| Ответ | При слиянии капель освобождается энергия Дж. |
ПРИМЕР 3
| Задание | Определить коэффициент поверхностного натяжения масла, плотность которого равна , если при пропускании через пипетку масла получено 304 капли. Диаметр шейки пипетки 1,2 мм. |
| Решение | Капля масла отрывается от пипетки, когда сила тяжести равна силе поверхностного натяжения: |